Combinar una dosis de AstraZeneca con otra de Pfizer es eficaz y seguro
El ensayo, promovido por el Instituto de Salud Carlos III, señala que vacunar con una segunda inyección de Pfizer/BioNTech tras recibir la primera de Oxford/AstraZeneca genera una respuesta inmunitaria eficaz y segura. Los efectos adversos reportados son similares a los esperados en una vacunación estándar, de poca gravedad y corta duración.
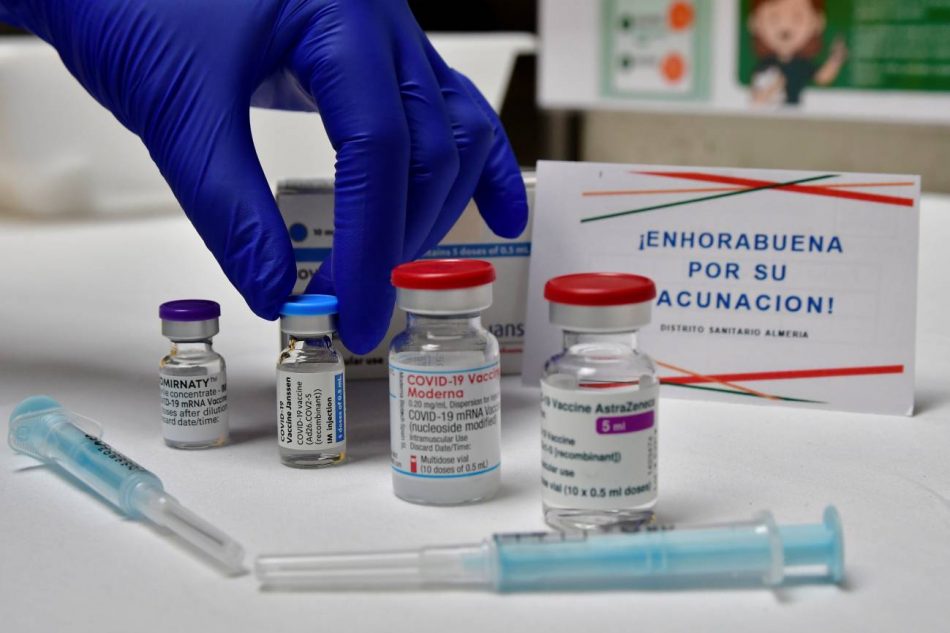
Administrar una segunda dosis de vacuna de Pfizer/BioNTech a una persona que recibió una primera vacuna de Oxford/AstraZeneca es seguro y eficaz, según los resultados preliminares del ensayo clínico CombivacS, que promueve el Instituto de Salud Carlos III (ISCIII). Los investigadores están estudiando la respuesta del sistema inmunitario (inmunogenicidad) y la seguridad (reactogenicidad), al combinar vacunas contra la covid-19 de diferentes tecnologías, lo que se denomina una pauta heteróloga frente al SARS-CoV-2.
Según los datos aportados en rueda de prensa telemática, los participantes que recibieron una segunda dosis de Pfizer presentaron más anticuerpos neutralizantes del SARS-CoV-2 que el grupo control del ensayo, que no recibió ninguna segunda dosis. Además, las reacciones adversas en los que recibieron una segunda vacuna eran de tipo leve a moderado y similares a las de una vacunación homogénea con Pfizer, como dolor en la zona de la inyección (88,2 %), cefalea (44,4 %), malestar general (41,7 %), induración local (35,5 %), eritema local (31 %) y escalofríos (25,4 %). La mayoría de síntomas desaparecía a partir del tercer día tras la vacunación y ninguna persona requirió de hospitalización.
El ISCIII ha presentado los resultados preliminares de CombivacS, en el que participan 673 personas menores de 60 años que ya han recibido una primea dosis de Vaxzevria (Oxford/AstraZeneca). De ellas, 441 personas forman parte del grupo experimental del ensayo, que recibirán una segunda inyección de Comirnaty (Pfizer/BioNTech) y a las que se le hace un seguimiento temporal tras la administración: siete días después, 14 días, 28 días, tres meses, seis meses y un año. Los que se han hecho públicos este martes son los del corte de dos semanas de estudio. El grupo control, por otro lado, lo conforman 232 personas.
Datos de inmunogenicidad
Para calcular los niveles de anticuerpos neutralizantes del SARS-CoV-2 en los participantes, se utilizaron tres técnicas diferentes: dos para calcular los anticuerpos IgG según la región de unión al receptor del SARS-CoV-2 y una tercera para confirmar que estos IgG neutralizaban el coronavirus, explicó la responsable del Laboratorio de Serología del Centro Nacional de Microbiolología, Maria Teresa Pérez Olmedo.
En los cálculos de nivel de anticuerpos, se confirmó que quienes recibieron una segunda dosis se multiplicaron notablemente a los siete días de la administración y siguieron aumentando a partir del día 14. Por el contrario, los anticuerpos en el grupo control permanecieron en niveles similares durante todo este tiempo.
Por otro lado, para confirmar que esos anticuerpos sí eran eficaces contra el coronavirus, se estudió el suero de pacientes del grupo experimental y se le ‘enfrentó’ con pseudovirus que portaban la proteína Spike del SARS-CoV-2. Este proceso, denominado ensayo de neutralización, arrojó buenos resultados y señaló un aumento en los niveles de anticuerpos siete veces mayor que en el grupo control.
Sobre esto último, Pérez Olmedo reiteró que este aumento es superior al esperado con otras pautas homólogas de vacunación: “con dos dosis de AstraZeneca, por ejemplo, el incremento es de unas tres veces, a diferencia de nuestro estudio en el que se ve un incremento de hasta siete veces”.
Reacciones adversas
Para conocer la reactogenicidad, los participantes tenían que contestar a un cuestionario de síntomas y efectos adversos que percibían después de la vacunación y valorarlos por ellos mismos por la intensidad percibida: leves, moderados o graves.
Los síntomas locales reportados más frecuentes son dolor en la inyección (88,2 %), induración (35,5 %), eritema (31 %), exantema (15 %) y prurito (10,9 %). Los sistémicos más comunes, por otro lado, son cefalea (44,4 %), malestar general (41,7 %), escalofríos (25,4 %), náuseas (10,9 %), tos (7,4 %) y fiebre (2,5 %). La mayoría de estos síntomas aparecieron a las 24 horas después de la inyección y desaparecieron prácticamente a partir del tercer día.
Según la intensidad percibida, el 68,3 % de los participantes los consideraban como leves, el 30 % como moderados y solo un 1,75 % afirmaban que eran intensos. No obstante, los síntomas de este último grupo eran malestar general, mialgias, cefalea y artralgias, que no revisten gravedad. Por último, ningún caso requirió de hospitalización.
“Todos estos datos de reacciones adversas son muy similares a los de un ensayo clínico en fase III de Comirnaty, casi superponibles”, declaró Magdalena Campins, jefa de Medicina Preventiva y Epidemiología del Hospital Vall d’Hebrón de Barcelona.
Cuestionados por los periodistas sobre la discrepancia entre los datos de reactogenicidad de este ensayo y los del británico Com-CoV, que se publicaron la semana pasada y que sí denotaban más reacciones adversas leves, Campins ha respondido que las diferencias entre ambos estudios tienen que ver con los diseños de cada uno: “El suyo pueden comparar hasta cuatro brazos [combinaciones de pauta de vacunas] diferentes y nosotros solo una, además que analizamos diferentes grupos de edad y administramos las dosis en semanas diferentes. No son estudios comparables”, ha subrayado.

Presentación de resultados preliminares en la sede del ISCIII. / Ministerio de Ciencia e Innovación
Detalles del estudio
CombivacS es el primer estudio mundial que hasta el momento ofrece datos sobre inmunogenicidad derivada del uso combinado de dos vacunas distintas. El estudio británico Com-CoV, que también alterna dos vacunas, solo ha publicado datos preliminares de reactogenicidad. El estudio del instituto público español es un ensayo clínico en fase II aleatorizado, multicéntrico y con proporción 2:1, esto es, que por cada participante de grupo control hay dos participantes del grupo experimental.
El ensayo seguirá en desarrollo en cinco hospitales vinculados a Institutos de Investigación Sanitaria como son Cruces en Vizcaya, La Paz y Hospital Clínico San Carlos de Madrid; el Vall d’Hebron y el Clínic, de Barcelona. Por su parte, el Centro Nacional de Microbiología (CNM) del ISCIII actúa como laboratorio central.
Los datos del estudio han sido analizados por un comité independiente de seguridad, que ha aconsejado proceder con la vacunación de las personas del grupo control con la segunda dosis de Comirnaty, según preveía el ensayo si se cumplían las hipótesis de inmunogenicidad y reactogenicidad previstas. También se comunicarán los resultados preliminares a la comunidad científica y a las autoridades sanitarias.


